Il dolore lombare (LBP) è una condizione comune che può derivare da una varietà di cause, tra cui i danni ai dischi intervertebrali (IVD). È una sensazione spiacevole associata a lesioni reali o potenziali ai tessuti. La degenerazione del disco è una delle cause più comuni di LBP, in particolare nella regione lombosacrale. Il LBP può manifestarsi con sintomi meccanici, come il dolore associato al carico e a determinate posture (ad esempio, stando in piedi o seduti per lungo tempo o trasportando un carico pesante), ma può anche essere accompagnato da dolore irradiato verso gli arti inferiori (radicolopatia).
Il LBP discogenico è un tipo specifico di dolore che origina dalla degenerazione dei dischi intervertebrali, e la sua patofisiologia è strettamente legata a cambiamenti degenerativi nei dischi stessi. Il dolore può derivare da vari meccanismi, tra cui la compressione nervosa, la proliferazione delle fibre nervose nel disco e l’infiammazione. Inoltre, la degenerazione discale spesso porta a una diminuzione dell’altezza del disco, a cambiamenti nel comportamento del nucleo polposo (NP) e dell’anulus fibrosus (AF), e alla formazione di osteofiti.
Anatomia dei dischi intervertebrali
Il disco intervertebrale (IVD) tra le vertebre adiacenti è un’articolazione cartilaginea secondaria (sinfisi). Unisce le vertebre adiacenti in una colonna semirigida continua, importante per il movimento e per la distribuzione del carico. Ogni IVD è composto da un anulus fibroso (AF) esterno e un nucleo polposo (NP) centrale e gelatinoso. Il nucleo è situato tra la placca epifisaria ialina (CEP) delle vertebre.
Anulus Fibroso (AF)
L’AF è un anello fibroso composto da 15 a 25 strati concentrici di fibre di collagene altamente organizzate, chiamati lamelle, che circondano il NP. Ogni lamella è formata da fibre di collagene robuste che corrono obliquamente, con un angolo di circa 30° da una vertebra all’altra. Le fibre delle lamelle adiacenti si incrociano obliquamente in direzioni opposte, con angoli superiori ai 60°. Questa disposizione consente una rotazione e una flessione limitata tra le vertebre adiacenti e permette all’IVD di sopportare carichi circonferenziali . L’AF contiene il 65-70% di acqua e il suo peso secco è composto per circa il 20% da proteoglicani, per il 50-70% da collagene e per il 2% da elastina. Lo spessore di ogni lamella varia da 100 a 500 µm, con le lamelle esterne più spesse rispetto a quelle interne. Inoltre, ogni lamella è separata da un tessuto interlamellare contenente una matrice ricca di proteoglicani, fibre elastiche e cellule. L’AF può essere ulteriormente diviso in due zone: l’AF interno contiene principalmente fibre di collagene di tipo II prodotte da cellule simili a condrociti di forma rotonda. Al contrario, l’AF esterno contiene principalmente fibre di collagene di tipo I prodotte da cellule allungate e fusiformi simili ai fibroblasti di origine mesenchimale.
Nucleo Pulposo (NP)
Il NP è il nucleo dell’IVD. Contiene dal 70 al 90% di acqua, mentre il suo peso secco è composto per circa il 35-65% da proteoglicani, per il 5-20% da fibrille di collagene di tipo II fine e il restante peso secco è costituito da alcune proteine non collagene e elastina. Il contenuto elevato di acqua del NP è mantenuto dai proteoglicani e distribuisce la pressione idraulica alla matrice extracellulare (ECM), alleviando lo stress sull’IVD. Il contenuto cellulare del NP consiste in una miscela di grandi cellule notocordali e di cellule mesenchimali più piccole simili ai condrociti. Le cellule notocordali, grandi e altamente vacuolate, subiscono modifiche morfologiche e funzionali, trasformandosi in cellule simili ai fibrocondroblasti man mano che l’IVD matura. Poiché le lamelle dell’AF sono più sottili nella parte posteriore rispetto a quelle nella parte anteriore e laterale dell’IVD, il NP si trova tra il centro e la parte posteriore dell’IVD.
Piastra Cartilaginea (CEP)
La CEP è costituita da sottili strati di cartilagine ialina (circa 0,6 mm di spessore) che collegano l’IVD superiormente e inferiormente ai corpi vertebrali adiacenti. Essa funge da barriera meccanica tra il NP e la vertebra, nonché da porta di trasporto per i nutrienti che entrano nell’IVD dai vasi sanguigni adiacenti. La CEP è legata debolmente al corpo vertebrale sottostante, rendendo la piastra vulnerabile alla separazione segmentale quando vengono applicati stress orizzontali eccessivi. La CEP è composta per circa il 60% da acqua, e i principali costituenti del peso secco sono il collagene di tipo II e i proteoglicani. Morfologicamente, la CEP contiene cellule allungate disposte parallelamente all’IVD in allineamento con le fibre di collagene, e le cellule producono una matrice interterritoriale ricca di collagene e una matrice territoriale ricca di proteoglicani.
Vascolarizzazione e innervazione
L’IVD è uno dei tessuti avascolari, che riceve solo piccole arterie che irrorano le fibre periferiche più esterne dell’AF. Pertanto, le altre componenti dell’IVD dipendono dalla fornitura di nutrienti e ossigeno e dall’eliminazione dei rifiuti dai vasi sanguigni sottostanti la CEP e dalle fibre periferiche dell’AF. Numerosi cambiamenti patologici, in particolare nella CEP, come la sclerosi ossea, le alterazioni del flusso sanguigno o la calcificazione della piastra terminale, possono influenzare il trasporto dai vasi sanguigni attraverso la CEP, il che porta alla morte cellulare nel NP, la componente dell’IVD più colpita poiché le sue cellule sono le più lontane dalle fonti di nutrimento. In generale, solo il terzo esterno dell’AF è innervato dai nervi sinuvertebrali (SVN), formati dall’unione di una radice somatica del ramo ventrale e una radice autonoma fornita dal ramo grigio. Il NP non ha innervazione nervosa
Meccanismi di Dolore Discogenico
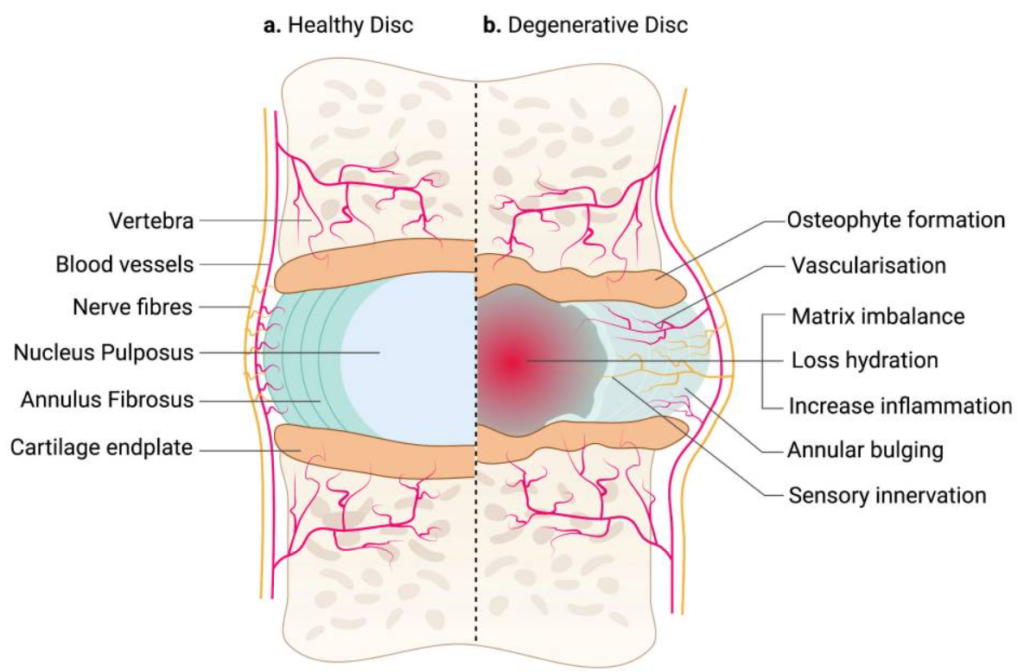
La degenerazione del disco intervertebrale (IVD) è un processo multifattoriale che porta a cambiamenti strutturali nel disco, tra cui perdita di idratazione, alterazione nella demarcazione tra NP e AF, e formazione di osteofiti. Questi cambiamenti strutturali, evidenti in immagini come la risonanza magnetica (MRI), favoriscono l’ingresso di fibre nervose nel disco (un fenomeno noto come nerve ingrowth), che è associato alla sensibilizzazione e al dolore.
In particolare, l’infiammazione gioca un ruolo cruciale in questo processo. Le citochine pro-infiammatorie come l’IL-1β stimolano l’espressione di neurotrofine come NGF (Nerve Growth Factor) e BDNF (Brain-Derived Neurotrophic Factor), che favoriscono la crescita delle fibre nervose sensoriali nel disco. Queste fibre nervose, che prima non erano presenti nei dischi sani, iniziano a produrre neuropeptidi come la sostanza P e il CGRP (peptide correlato al gene della calcitonina), che sono direttamente coinvolti nel processo di trasmissione del dolore.
Un altro fenomeno associato alla degenerazione discale è l’attivazione dei recettori nocicettivi sensibili a stimoli meccanici e a mediatori di danno tissutale, come la bradichinina, le prostaglandine, l’istamina e i leucotrieni. Questi recettori, tra cui quelli appartenenti alle fibre Aδ e C, rispondono a stimoli dannosi, generando segnali di dolore che vengono trasmessi al sistema nervoso centrale.
Vie Nocicettive: Sensibilizzazione Periferica e Centrale
La sensibilizzazione periferica e centrale è un aspetto fondamentale del dolore discogenico. In seguito all’infiammazione e all’ingresso nervoso nel disco, le fibre Aδ e C sensoriali si sensibilizzano, aumentando la loro capacità di trasmettere segnali dolorosi. Questo processo coinvolge anche il cambiamento fenotipico delle fibre Aβ, che, in risposta all’infiammazione, iniziano ad assumere caratteristiche simili a quelle delle fibre C, amplificando ulteriormente la trasmissione del dolore.
Le vie nocicettive sono strutturate in modo tale che le fibre sensoriali Aδ e C proiettano al corno dorsale del midollo spinale, in particolare nelle lamine I e II. Da lì, il dolore viene trasmesso al talamo e successivamente alla corteccia cerebrale per l’elaborazione cosciente. Questo processo di trasmissione è modulato da recettori ionotropici come i recettori AMPA e NMDA, che vengono attivati da neurotrasmettitori eccitatori come il glutammato. La sensibilizzazione centrale è mediata anche da neurotrofine come il BDNF, che potenzia la trasmissione sinaptica, amplificando la percezione del dolore.
Neurotrasmettitori e Mediatori del Dolore
I principali neurotrasmettitori coinvolti nel dolore discogenico sono glutammato, sostanza P, CGRP e neurokinine. Il glutammato è il neurotrasmettitore primario che media la trasmissione del dolore, agendo sui recettori AMPA e NMDA. L’attivazione dei recettori NMDA in particolare è fondamentale per la plasticità sinaptica, un processo che contribuisce alla sensibilizzazione del sistema nervoso centrale al dolore.
Le neurotrofine come NGF e BDNF sono cruciali per la crescita nervosa e la sensibilizzazione al dolore. Queste molecole stimolano il rilascio di glutammato e neuropeptidi da parte dei neuroni presinaptici e modulano la funzione dei recettori del dolore, come i recettori CGRP e NK1/NK2. Il potenziamento della trasmissione sinaptica attraverso questi recettori aumenta l’eccitabilità delle cellule postsinaptiche e amplifica la percezione del dolore.
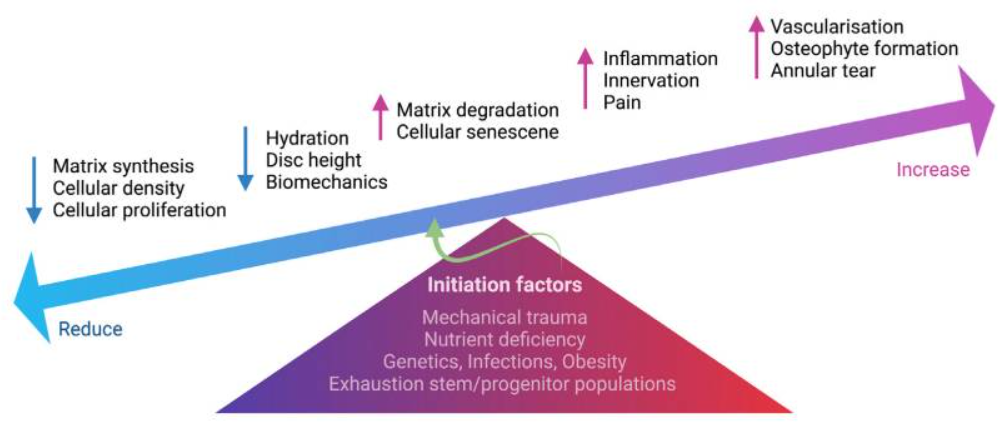
FONTE: Discogenic Low Back Pain: Anatomy, Pathophysiology and Treatments of Intervertebral Disc Degeneration – Isma Liza Mohd Isa, Seong Lin Teoh, Nurul Huda Mohd Nor, Sabarul Afian Mokhtar
https://pmc.ncbi.nlm.nih.gov/articles/PMC9820240/

👨⚕️ Affidarsi a un Osteopata professionista significa prendersi cura di sé a un livello profondo, avanzando nel percorso verso l’armonia interiore e nel miglioramento della salute complessiva.

